エビデンス(EBM)を実践するにあたりたくさんの論文を読む必要があります。
その多くの論文・情報の中からすべての情報が正しいとは言えません。
よって、その情報が正確なのか吟味する必要があります。
エビデンスには5つのステップがあり、ステップ3では収集した情報を
批判的吟味する過程が必要となります。
今回はランダム化比較試験の研究の質(内的妥当性)をどのように評価
していくのを解説します。
ランダム化比較試験のチェック項目
ランダム化比較試験の流れとチェック項目
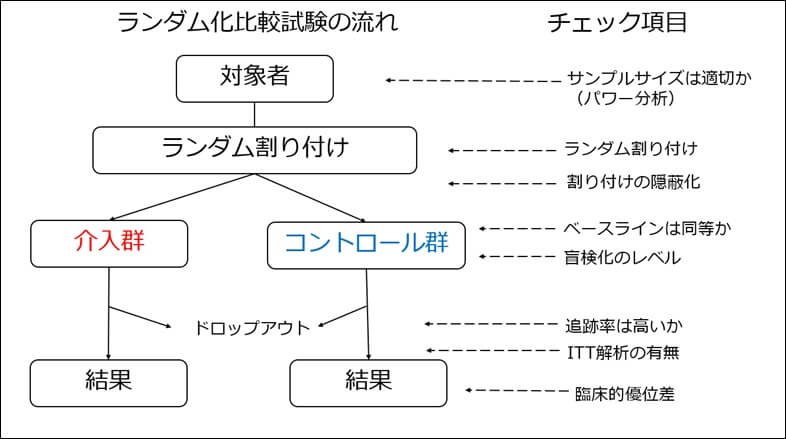
- ランダム割り付け:対象は比較する群に無作為に割り当てられているか
- 割付の隠蔽:比較する群への割り当ての仕方は隠されたか
- ベースライン:比較した群間のベースラインは同様であるか
- 対象者・評価者・治療者への盲検化:盲検化はされたか
- フォローアップ率:割り付け時の対象者の85%以上が介入効果の判定対象となっているか
- ITT解析:治療企図解析(ITT解析)がされているか
- 症例数:サンプルサイズは十分か
- 臨床的優位差:統計学優位でかつ臨床的にも優位か
一つ一つなぜチェックするべきかを説明していきます。
ランダム割り付け
対象者がランダム割り付けされてるか確認しましょう。
母集団をランダムに介入群とコントロール群に割り付けることで
治療以外の要素を平等にすることができます。
選択バイアスの影響を少なくするメリットがあります。
割付の隠蔽化
対象者を各群に割り付ける担当者にランダム割り付け表が隠蔽化
されていたのかを確認しましょう。
隠蔽化されていない場合、参加者がどちらのグループに割り付けされるか
分かってしまうため、症状が重い・症状が軽い患者を都合が良いグループに
割り振ってしまう可能性があります。
選択バイアスの影響を少なくするメリットがあります。
ベースラインは同等か
ベースラインとは
研究開始時の対象者の年齢、性別、疾患の重症度といった背景因子
のことを呼びます。
ランダム割り付けされている研究では群間に差はないはずですが
本当に差がないのかを確認しましょう。
ベースラインが同等ではないと、背景因子が交絡因子となり研究結果に
影響を及ぼす可能性があります。
マッチングとも呼ばれるため、この記載があればベースラインは
同等にしたと解釈して良いです。
交絡バイアスの影響を少なくするメリットがあります。
対象者・評価者・治療者への盲検化
盲検化とはブラインディングまたはマスキングとも呼ばれています。
データ収集・解析の過程で対象者、治療者、結果の評価者、データ解析者へ
情報を伏せる手法です。
一人一人の患者がどんな治療を受けているのか治療者や評価者は
知らないことが望ましいのです。
盲検化のレベル
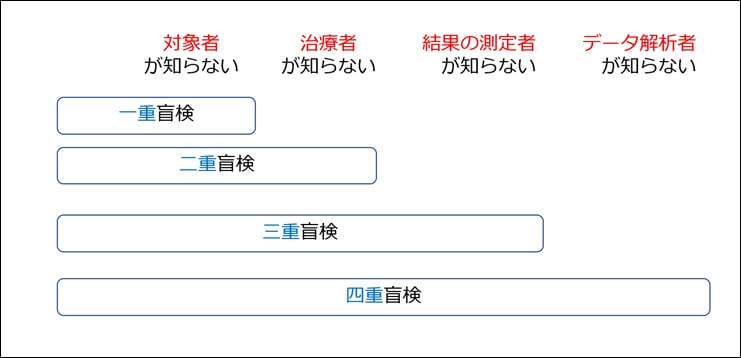
情報・測定バイアスの影響を少なくするメリットがあります。
フォローアップ率(追跡率)は十分か
理想的には研究開始時から終了時まで全ての患者のデータが
解析できることであるが、途中で患者が脱落(ドロップアウト)
するケースが度々生じます。
ドロップアウトが多く、フォローアップ率が低いと
以下の2つの問題が生じます。
〇せっかく最初にランダムに割り付けてベースラインを同等にしたのに
最後にはベースラインに偏りが生じてしまう。
〇症例数が減ることで信頼性・再現性が乏しくなってしまう。
一般的にはフォローアップ率(追跡率)は
80%~85%が妥当であると言われています。
ITT解析されているか
ITTとはIntention To Treatの略であり、「意図された通りの治療」の意味となります。
ITT解析とは研究の初めに割り付けた治療群・コントロール群を研究終了時にも
変えずに解析する手法です。
ITT解析の目的はランダム割り付けの保持です。
せっかく最初にランダムに割り付けたの、途中で片方のグループの
ドロップアウトの数が多い場合、ベースラインに偏りが出来てしまうため
研究終了後もドロップアウトした患者を含めてITT解析していきます。
症例数(サンプルサイズ)は適切か
研究を開始するにあたり、仮説を検証して結果を証明するためには
適切なサンプルサイズが必要となります。
サンプルサイズを決める方法はパワー分析と呼ばれます。
論文の本文でパワー分析したと記載があればサンプルサイズを
事前に決めた状態で研究を開始したと考えていいでしょう。
サンプルサイズは多すぎても少なすぎても問題が生じます。
サンプルサイズが多い場合
統計学的優位差が生じやすくなります。
N数(母集団)が増えるほど、優位になりやすということです。
サンプルサイズが少ない場合
本当は差があるのに統計学的な有意差が生じなくなる。
N数(母集団)が少ないと、優位差が出ずらいということです。
よってパワー分析されているのかを確認しましょう。
臨床的優位差
臨床的優位差とは「臨床的に意義のある優位な差のこと」です。
統計学的に優位差がでたからといって臨床的に優位とは限りません。
文献を読むと「P値が0.05を満たしたため両群間で優位差あり」と
記載してあるのを見かけると思います。
しかし、統計学的優位なだけで、どのくらい効果があったのかを
確認する必要があります。
例えば
P(患者):腰痛がある人
I(介入):ストレッチと体幹筋力トレーニングの併用
C(コントロール):体幹筋力トレーニング単独
O(アウトカム):VAS
このような論文があったとして
最終的にストレッチと体幹筋力トレーニングを行った方が
P値 0.05を満たして優位に痛みが改善したと結論づけた論文を読む際
VASの改善が100mmの中で介入群は40mm改善、コントロール群は38mm改善
その差はわずが0.2mmとなります。
この差が臨床的優位であるかを吟味する必要があります。
臨床的に優位かどうなのかを判断するにはMCIDが重要となります。
MCIDとはMinimal Clinically Important Differenceの略であり、
臨床的に意味のある最小変化量のことを呼びます。
簡単に言うと治療前後でアウトカムが〇〇点の改善すれば
臨床的に意味のある差であると定義して良いという指標になります。
MCIDは患者の背景やアウトカムの指標によっても変わってくるので
論文を読む際はこのアウトカムのMCIDは何点だろうかと
意識して読むことが重要となります。
最近ではMCIDの重要性が認識され始めて
海外の論文ではアウトカムがMCIDを満たしたかどうかを
考察で記載してある論文もあります。
アウトカムのMCIDが分からない際はインターネットで調べるか、
筆者はこちらのサイトを使ってMCIDは何点なのか確認しています。
臨床的に優位かはMCIDを満たしているのかを確認しましょう。
系統的な評価ツール
系統的な研究の質の評価にはペドロスケールとRAAMBOが
分かりやすくて使いやすいと思います。
ペドロスケールでの評価

GATEフレーム(RAAMBO)での評価

まとめ
今回はランダム化比較試験の批判的吟味の方法を紹介しました。
チェックする項目がたくさんあり慣れるまでは時間がかかると思います。
慣れてくると論文のこの箇所にこの項目が書いてるのではと予想しながら
読めるので読むペースが早くなってくるはずです。
批判的吟味はエビデンスの5ステップのステップ3で必ず重要となるため
この機会にぜひ、論文を読む際は意識して読んでみて下さい。
統計学について体系的に学びたいかたは対馬 栄輝 先生が講義している
オンラインセミナー リハノメがおすすめです。
第12回までにわたっての講義が視聴可能です。
統計学の基本からリハビリへの活かし方など幅広く学べると思います。
リハノメについてはこちらのブログに詳しく書いてあります。




コメント